Хімія. Уроки. 9 клас
Посібник містить календарно-тематичне планування із визначенням очікуваних результатів навчання та наскрізних змістових ліній, а також конспекти уроків із хімії за оновленою навчальною програмою для 9-го класу.
Усі уроки відповідають методичним і дидактичним вимогам нової української школи, адже спрямовані на розвиток пізнавальної активності учнів і максимальну інтеграцію навчання в життя.
Посібник стане в пригоді вчителям хімії загальноосвітніх і професійно-технічних навчальних закладів, викладачам методики навчання хімії у ВНЗ, студентам хімічних спеціальностей педагогічних університетів.
83,00 ₴
Немає в наявності
ЗМІСТ
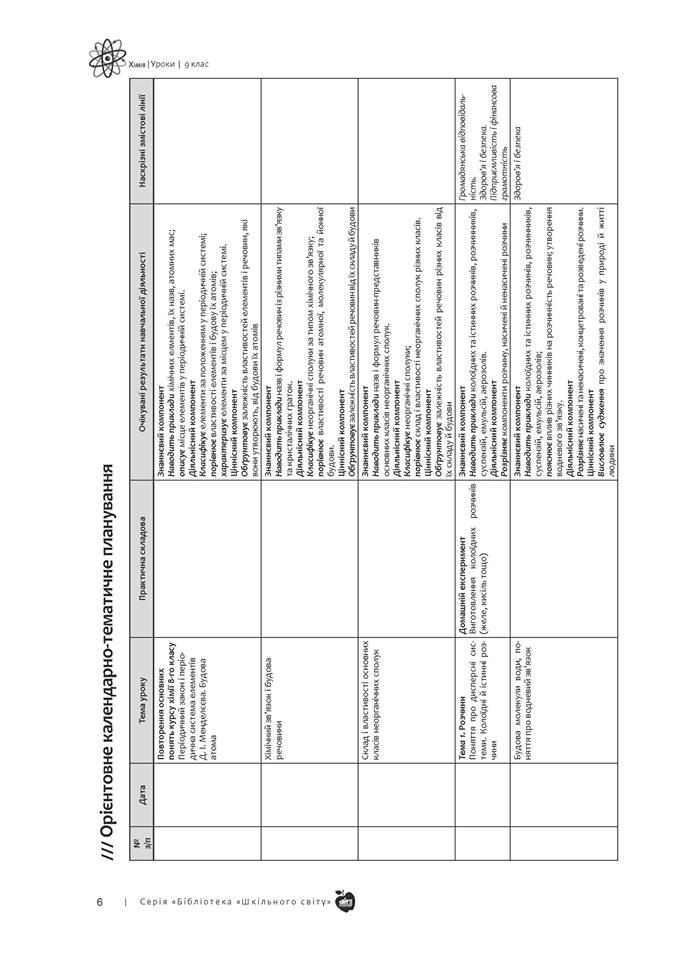
Орієнтовне календарно-тематичне планування
- Урок 1. Періодичний закон і періодична система хімічних елементів. Будова атома
- Урок 2. Хімічний зв’язок і будова речовини
- Урок 3. Основні класи неорганічних сполук
- Урок 4. Хімічні властивості основних класів неорганічних сполук
- Урок 5. Поняття про дисперсні системи. Колоїдні й істинні розчини
- Урок 6. Будова молекули води. Поняття про водневий зв’язок
- Урок 7. Розчинність речовин, її залежність від різних чинників
- Урок 8. Розчинення як фізико-хімічний процес. Кристалогідрати
- Урок 9. Розв’язування задач за рівняннями реакцій із використанням розчинів із певною масовою часткою розчиненої речовини
- Урок 10. Електролітична дисоціація. Електроліти й неелектроліти
Читати далі
- Урок 11. Електролітична дисоціація кислот, основ і солей у водних розчинах
- Урок 12. Ступінь дисоціації. Сильні та слабкі електроліти
- Урок 13. Виявлення в розчині гідроксид-іонів і йонів Гідрогену
- Урок 14. Поняття про рН розчину. Значення рН для характеристики кислотного чи лужного середовища
- Урок 15. Реакції обміну між розчинами електролітів. Йонні рівняння
- Урок 16—17. Йонно-молекулярні рівняння хімічних реакцій
- Урок 18. Якісні реакції на деякі йони. Застосування якісних реакцій
- Урок 19. Практична робота 1. Реакції йонного обміну між електролітами у водних розчинах
- Урок 20. Практична робота 2. Розв’язування експериментальних задач
- Урок 21. Розв’язування розрахункових задач
- Урок 22. Контрольна робота 1 із теми «Розчини»
- Урок 23—24. Узагальнення знань із теми «Розчини». Значення розчинів у житті людини та суспільства.Захист проектів
- Урок 25. Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну
- Урок 26. Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки
- Урок 27. Складання формули сполуки за відомими ступенями окиснення елементів
- Урок 28. Окисно-відновні реакції. Процеси окиснення і відновлення, окисники та відновники
- Урок 29. Складання рівнянь окисно-відновних реакцій
- Урок 30. Значення окисно-відновних реакцій у природі й діяльності людини
- Урок 31. Екзотермічні й ендотермічні реакції. Термохімічне рівняння
- Урок 32. Оборотні й необоротні реакції
- Урок 33. Швидкість хімічної реакції, залежність швидкості реакції від різних чинників
- Урок 34. Практична робота 3. Вплив різних чинників на швидкість хімічних реакцій
- Урок 35. Самостійна робота 2 із теми «Хімічні реакції»
- Урок 36. Узагальнення з теми «Хімічні реакції»
- Урок 37. Особливості органічних сполук
- Урок 38. Метан як представник насичених вуглеводнів
- Урок 39. Гомологи метану
- Урок 40. Етилен і ацетилен як представники ненасичених вуглеводнів
- Урок 41. Обчислення об’ємних відношень газів за хімічними рівняннями
- Урок 42. Поняття про полімери на прикладі поліетилену
- Урок 43. Природні джерела вуглеводнів. Застосування вуглеводнів
- Урок 44. Поняття про спирти. Етанол: молекулярна і структурна формули, фізичні та хімічні властивості
- Урок 45. Гліцерол: молекулярна і структурна формули, фізичні та хімічні властивості. Якісна реакція на гліцерил
- Урок 46. Отруйність спиртів. Згубна дія алкоголю на організм людини
- Урок 47. Етанова (оцтова) кислота: склад і фізичні властивості
- Урок 48. Хімічні властивості та застосування етанової кислоти. Поняття про вищі карбонові кислоти
- Урок 49. Практична робота 3. Властивості етанової кислоти
- Урок 50. Жири, їх склад і властивості. Мило, його склад, мийна дія. Біологічна роль жирів
- Урок 51. Вуглеводи: глюкоза та сахароза. Їх будова, властивості, поширення в природі
- Урок 52. Крохмаль і целюлоза — природні полімери. Їх будова, властивості, поширення в природі
- Урок 53. Застосування вуглеводів, їх біологічна роль
- Урок 54. Нітрогеновмісні органічні сполуки. Амінокислоти
- Урок 55. Білки як біологічні полімери. Біологічна роль амінокислот і білків
- Урок 56. Природні й синтетичні органічні сполуки
- Урок 57. Захист довкілля від стійких органічних забруднювачів
- Урок 58. Практична робота 4. Виявлення органічних сполук у харчових продуктах
- Урок 59. Контрольна робота з теми «Початкові поняття про органічні сполуки»
- Урок 60. Багатоманітність речовин і хімічних реакцій
- Урок 61. Взаємозв’язки між речовинами та їх взаємоперетворення
- Урок 62. Місце хімії серед наук про природу, її значення для розуміння наукової картини світу
- Урок 63. Роль хімічної науки для забезпечення сталого розвитку людства
- Урок 64. Хімічна наука та виробництво в Україні. Відомі вітчизняні вчені — творці хімічної науки
- Урок 65. Підсумковий урок із теми «Роль хімії в житті суспільства»
Тільки покупці, які увійшли на сайт і вже купили цей товар, можуть залишати відгуки.














Відгуки
Відгуків немає, поки що.